12-26 23:18:37 浏览次数:142次 栏目:高考化学复习资料
②实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由________________________________。
www.quxue6.com
(3)某温度下,将0.1 mol CO和0.3 mol H2充入10L的密闭容器内发生反应CO(g)+3H2(g) 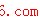 CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)
CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)
【分析】平衡题目中规中矩,老“盖斯”又出现了。第一问书写热化学方程式用我们一直强调的“待定系数法”即可。
另外,一定要毫无保留的细心,除了计算外还要注意注意书写热化学方程式中的常见错误:①丢掉状态,②△H符号丢掉( +/-都不能丢 ) ③单位写错(正确为KJ/mol )。
最后一问考察的三段式,这种每年必考保分的题目你真的好意思做错吗?做错的盆友请自行了断。需要强调,平衡常数K需注明单位!最后,再多说一句“计算结果保留两位有效数字”,这种小细节在做题的时候一定要注意,我们说过,看到类似话就要条件反射“画圈圈”。
【答案】
(1)CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH=-162kJ·mol-1 (3分,热化学方程式2分,数据1分)
CH4(g)+2H2O(g) ΔH=-162kJ·mol-1 (3分,热化学方程式2分,数据1分)
(2)①< (3分)
②相对于N点而言,采用M点,温度在500-600K之间,温度较高,反应速率较快,氢气的平衡转化率也较高,压强为常压对设备要求不高。 (3分)
③(7分)

32.(16分)锰是冶炼工业中常用的添加剂。以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:

已知25℃,部分物质的溶度积常数如下:
物质
Mn(OH)2
Co(OH)2
Ni(OH)2
MnS
CoS
NiS
Ksp
2.1×10-13
3.0×10-16
5.0×10-16
1.0×10-11
5.0×10-22
1.0×10-22
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是 。
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,反应的离子方程式是 ,加氨水调节溶液的pH为5.0-6.0,以除去Fe3+。
(3)步骤Ⅲ中,滤渣2的主要成分是 。
(4)步骤Ⅳ中,在 (填“阴”或“阳”)极析出Mn,电极反应方程式为 。
(5)电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。进行二级沉降的目的是 。
【分析】“工艺流程框图+溶度积表”是经典模型啊有木有!课上练了不止5次啊有木有!!如果你依然倔强的说老湿我还是看不懂这个流程。那么,盆友,你至少也能拿到一半的分数。因为前两问只是方程式的书写,与流程无关。根据已有知识书写未学过的方程式
,2017年广州市高三调研考化学卷点评tag: 化学 广州市 高考化学复习资料,高考化学复习资料大全,高考化学基础知识,高中学习 - 高考复习 - 高考化学复习资料